Un equipo de investigadores chinos demuestra por primera vez la viabilidad de desarrollar un órgano sólido humano en el organismo de otra especie.
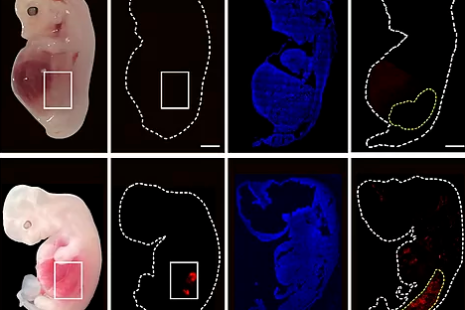
Los riñones contienen un 50-60% de células humanas y crecieron con normalidad en los animales hasta que se interrumpió la gestación a los 25-28 días. Este experimento, que se publica en Cell Stem Cell, demuestra la viabilidad de cultivar un órgano sólido humano en el interior de otra especie. Los investigadores no solo lograron las quimeras con éxito sino que además mostraron que los riñones crecían con una estructura normal.
Este experimento supone un hito científico. Los responsables son un equipo de investigadores de la Universidad de Cantón, en China. «Nuestro estudio demuestra que órganos humanos sólidos como el riñón pueden crecer en embriones de cerdo y esto es muy emocionante, porque las implicaciones son inmensas», escribe a este medio desde China el inmunólogo español Miguel A. Esteban, quien es uno de los autores principales del estudio.
Las implicaciones a las que alude el científico son un viejo sueño de la medicina para encontrar fórmulas que permitan «cultivar» en animales órganos humanos disponibles para el trasplante.
La integración de células de diferentes especies ha sido una importante barrera en esas investigaciones. Ahora este equipo de científicos de los Institutos de Biomedicina y Salud de Cantón, de la Academia China de Ciencias, la ha superado con un procedimiento que incluye la técnica de edición genética CRISPR. Con ella eliminaron en el embrión porcino dos genes necesarios para que se forme el riñón, y de esta forma crearon una especie de nicho para que las células humanas no tuvieran que competir con las porcinas.
¿CÓMO HAN CONSEGUIDO ‘CULTIVAR’ LOS ÓRGANOS?
Después, prepararon células madre pluripotentes humanas a la que administraron factores que favorecieran su supervivencia y que cultivaron en un medio optimizado, hasta lograr unas células similares a las embrionarias humanas. Una vez integradas en los embriones porcinos, cultivaron esas quimeras bajo condiciones óptimas de nutrientes y señales específicas tanto para las células humanas como para las porcinas, y, finalmente, implantaron los embriones en las cerdas.
En total, transfirieron 1.820 embriones a 13 hembras. El proceso se interrumpió a los 25 ó 28 días para determinar el estado de los riñones humanizados. En cinco embriones analizados los científicos comprobaron que los órganos resultaron estructuralmente normales para su fase de desarrollo -se encontraban en fase de mesonefros y habían formado túbulos y brotes celulares que se convertirían en uréteres para conectar riñón con vejiga- y que estaban compuestos por un 50-60% de células humanas.
«El riñón que desarrollamos no era un riñón maduro, para ello habría que prolongar la gestación. Es posible que otro tipo de barreras técnicas dificulten la maduración, pero estamos trabajando en ello», comenta Miguel A. Esteban, que lleva 16 años trabajando como investigador científico en China.
Una de las complicaciones que pueden echar al traste el procedimiento es que las células humanas invadan otros tejidos u órganos, algo que en el experimento no ocurrió, al menos no en proporciones preocupantes. «Vimos muy pocas células neuronales humanas en el cerebro y la médula espinal y ninguna célula humana en la cresta genital, lo que indica que las células madre pluripotentes humanas no se diferenciaron en células germinales», aclara el autor principal Zhen Dai, del Instituto de Biomedicina y Salud de Guangzhou.
No obstante, matiza Miguel A. Esteban, «para asegurarnos de que esto no ocurre en absoluto estamos modificando las células humanas y así solo se diferenciarán en el órgano o tejido deseado dentro del embrión de cerdo».
SIGUIENTES ÓRGANOS A DESARROLLAR: CORAZÓN E HÍGADO
«Estamos trabajando también en la formación de otros órganos humanos en cerdos, como el corazón o el hígado, y las investigaciones están muy avanzadas», añade. Este estudio sobre el riñón se ha desarrollado a lo largo de unos cinco años de trabajo, expone, realizado en colaboración con otros grupos, «en particular con los de Liangxue Lai y de Guangjin Pan en nuestro instituto».
No es la primera vez que se desarrollan embriones interespecie, pero sí que se consigue cultivar un órgano sólido humanizado en otro animal. Hasta ahora se había demostrado la viabilidad de integrar células humanas en embriones de otras especies.
Así lo demostraron las investigaciones pioneras del científicoJuan Carlos Izpisúa, fundador científico y director de los laboratorios Altos. En 2017, el grupo de Izpisúa, entonces en el Instituto Salk, en California, en colaboración con la Universidad Católica de Murcia publicó la prueba de concepto en Cell del desarrollo de células humanas en cerdos.
ASÍ QUEDAN LAS CÉLULAS ORGANIZADAS
El trabajo de la Universidad de Cantón continúa esa línea y como destaca Juan Carlos Izpisúa a este medio, «da un paso más allá» y «demuestra que las células humanas no sólo se integran, sino que también pueden organizarse espacialmente y contribuir a dos tejidos porcinos, el endotelio y el músculo esquelético. El estudio demuestra el desarrollo del mesonefros humano en otro mamífero mediante la complementación embrionaria temprana».
Para este experto, «probablemente, la siguiente etapa de esta apasionante línea de investigación sería comprobar si el primordio [células embrionarias que dan origen a un órgano] renal puede madurar hasta convertirse en metanefros [esbozo embrionario del riñón], algo técnicamente difícil ya que pueden aparecer otras barreras».
«Cultivar órganos humanizados maduros en cerdos aún no es posible, pero este estudio puede acercar un paso más la idea de que desarrollar órganos humanos en otros mamíferos es posible», afirma Juan Carlos Izpisúa.
El científico opina que los resultados representan «un gran paso adelante en este campo. No obstante, quedan muchos obstáculos por resolver; entre ellos: la coincidencia en el desarrollo entre las células donantes y las del hospedador dentro del embrión temprano, el tiempo diferencial de desarrollo, la competencia célula-célula (aunque esto se superó en buena medida en estos estudios) y la comunicación inadecuada célula porcina-célula humana».
Además, Izpisúa indica que «incluso antes de llegar al paso del trasplante, el cultivo de tejido humanizado en cerdos tiene un enorme potencial para el diseño de modelos de enfermedades, la investigación farmacológica, así como una mejor comprensión de la organogénesis humana».
Un objetivo compartido por los autores de este trabajo, quienes reconocen que emplear esta tecnología en el trasplante de órganos es un camino arduo que puede requerir aún muchos años, mientras que ven más cercano su uso como un método de estudio del desarrollo humano.