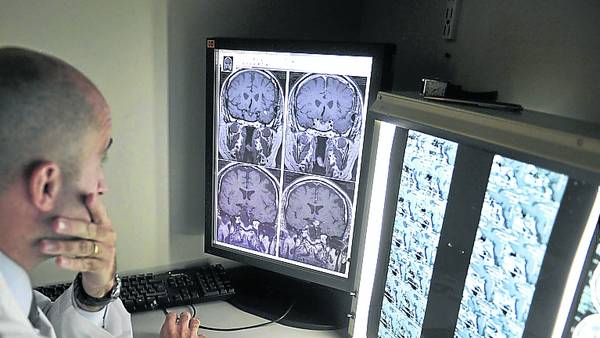
Mostraron que estaría vinculado con un desbalance en una proteína responsable de la maduración de las neuronas.
 El 25 de noviembre de 1901, el psiquiatra y neuropatólogo alemán Alois Alzheimer recibió a una paciente que lo haría célebre: Auguste Deter. Uno de sus síntomas era la pérdida de la memoria de corto plazo. Después de la muerte de Deter, en abril de 1906, Alzheimer analizó su historia clínica y estudió su cerebro. Fue así como pudo identificar «placas amiloides» (depósitos entre las neuronas) y «ovillos neurofibrilares» (conglomerados de una proteína intracelular llamada «tau») que se convertirían en los signos característicos de la enfermedad que hoy lleva su nombre.
El 25 de noviembre de 1901, el psiquiatra y neuropatólogo alemán Alois Alzheimer recibió a una paciente que lo haría célebre: Auguste Deter. Uno de sus síntomas era la pérdida de la memoria de corto plazo. Después de la muerte de Deter, en abril de 1906, Alzheimer analizó su historia clínica y estudió su cerebro. Fue así como pudo identificar «placas amiloides» (depósitos entre las neuronas) y «ovillos neurofibrilares» (conglomerados de una proteína intracelular llamada «tau») que se convertirían en los signos característicos de la enfermedad que hoy lleva su nombre.
«En la enfermedad de Alzheimer, la placa amiloide se deposita del lado de afuera de las neuronas y el ovillo neurofibrilar, del lado de adentro -explica Tomás Falzone, investigador adjunto del Conicet en el Instituto de Biología Celular y Neurociencia (IBCN) y coordinador de un equipo internacional que acaba de publicar en The Journal of Neuroscience un trabajo que describe el rol de tau en las enfermedades neurodegenerativas-. Pero la proteína tau no sólo está presente en el Alzheimer. También participa en la demencia frontal y en el mal de Parkinson.»
En su estudio, el equipo de investigadores argentinos, en colaboración con colegas de la República Checa y del Reino Unido, muestra que estos desórdenes pueden surgir de sutiles alteraciones en los niveles relativos de dos versiones de tau que existen naturalmente en el cerebro.
«Las neuronas producen varias formas de tau, especialmente dos llamadas 3R y 4R. Durante el desarrollo, hay niveles muy altos de 3R y muy bajos de 4R, pero en el cerebro adulto se equilibran en un 50% y 50% de cada una -dice Falzone-. Lo que se ve en enfermedades neurodegenerativas es una mayor proporción de una que de la otra.»
Las neuronas son las células más asimétricas del organismo. Tienen un cuerpo (soma), dendritas y una larga prolongación llamada axón. En el soma se sintetizan las proteínas, que luego son trasladadas al axón para ser usadas en la transmisión del impulso nervioso. Para llegar, se desplazan sobre un andamiaje constituido por unas estructuras tubulares que forman una especie de vía, los microtúbulos.
«Son como los durmientes del ferrocarril por el que viajan los nutrientes y los desechos de las neuronas -explica Gustavo Sevlever, director de docencia e investigación de Fleni, que no participó en el trabajo-. Cuando la proteína tau está alterada, no funcionan los durmientes y las vías se desarman.»
«Tau es una proteína con niveles de expresión muy regulados; mutaciones genéticas que influyen sobre estos mecanismos de regulación hacen que haya más de una que de la otra», explica Elena Avale, investigadora adjunta del Consejo en el Instituto de Investigaciones en Ingeniería Genética y Biología Molecular (Ingebi) y coordinadora del trabajo.
A lo largo de la investigación, Falzone y Avale trabajaron con neuronas humanas diferenciadas a partir de células madre. «Confirmamos que tuvieran la actividad eléctrica correspondiente, les regulamos la expresión de 3R y 4R, y encontramos que cuando en la célula madura se modifica la relación 50-50 entre ellas, aparecen defectos en el transporte sobre los microtúbulos -destaca Falzone-. Estos desbalances podrían estar en el origen de procesos neurodegenerativos como el Parkinson y ciertas demencias.»
«En el cerebro con Alzheimer hay dos proteínas anómalas -explica Sevlever-. La placa amiloide es extracelular y no correlaciona con el grado de demencia de los pacientes, por lo que se sospecha que podría ser un semáforo que indica que hay algún problema, pero que no es en sí mismo un agente tóxico. De hecho, los fármacos que se ensayaron hasta ahora limpiaron la placa amiloide, pero sin que el paciente mejorara. Aunque el PET permite verlo en vivo, sus resultados no son precisos: si no hay amiloide, es poco probable que haya Alzheimer; pero si hay, no es tan concluyente. La gran mayoría de los mayores de 85 tienen amiloide, tengan o no Alzheimer. La tau, por su parte, está en el interior de las neuronas. Aparece en el hipocampo en etapas muy tempranas y aparentemente es uno de los primeros signos de patología. Hoy hay dos maneras de detectarla: con una punción de líquido cefalorraquídeo o con PET, pero aunque empieza a haber algunos compuestos promisorios para identificarla, se usan en forma experimental y en muy pocos lugares del mundo. Probablemente, la correlación entre ambas sea el signo distintivo que delata estas enfermedades.»
Como todo indica que puede haber anomalías neuronales hasta 25 años antes de que se manifiesten los primeros síntomas, este hallazgo permitiría diseñar métodos de diagnóstico menos invasivos para detectar la proteína tau anómala. La estrategia también podría abrir la puerta a una terapia. «Nosotros generamos el desbalance y podríamos recuperarlo -indica Falzone-. Si se pudiera regular la síntesis de la proteína para que se mantenga la proporción 50-50, se podría corregir un número de patologías.»