Científicos españoles han probado con éxito una tecnología de organoides renales humanos con la que reparar los riñones y mejorar su viabilidad para el trasplante.
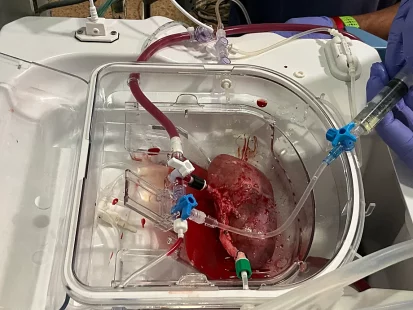
Los organoides, estructuras celulares diminutas que se asemejan a órganos humanos, es lo más cercano que hoy está la ciencia de fabricar un órgano en el laboratorio. Sin embargo, todavía no pueden considerarse un órgano completo, y por tanto, un recurso realista para poder solventar la escasez de órganos necesarios para el trasplante. Según datos de la Organización Nacional de Trasplantes (ONT), los injertos que se realizan a nivel global en el mundo apenas cubren un 10% de las necesidades de trasplante global.
Un equipo internacional de científicos, liderado por el Instituto de Bioingeniería de Cataluña (IBEC), en colaboración con el Instituto de Investigación Biomédica de A Coruña (INIBIC), propone una original estrategia para aplicar la tecnología de los organoides como una vía con la que aumentar los órganos disponibles, viables, para el trasplante, e incluso como una potencial terapia celular.
El experimento, cuyos detalles se acaban de publicar en la revista Nature Biomedical Engineering, ha consistido en producir organoides renales humanos por primera vez de manera escalable, en un número suficiente para un eventual uso terapéutico, y combinarlos con riñones de cerdo. Los riñones porcinos se extrajeron de los animales y se mantuvieron vivos conectados a una máquina de perfusión normotérmica, para después, ser reinjertados en los cerdos.
Esta prueba de concepto es fruto de una línea de investigación que inició en 2018 Núria Montserrat, investigadora ICREA en el IBEC en el momento del estudio y actual consejera del Departamento de Investigación y Universidades de la Generalidad de Cataluña, y que refleja el potencial de la medicina regenerativa y la bioingeniería de órganos.
Elena Garreta, investigadora senior del grupo de Pluripotencia para la regeneración de órganos del IBEC y co-primera autora del estudio, explica a este medio que el experimento demuestra por primera vez «la viabilidad de producir los organoides de manera escalable y segura. Hemos utilizado células de pluripotencialidad inducida humanas (iPS) que han sido sometidas a un proceso de diferenciación de 16 días, al cabo de los cuales conseguimos que se formaran los organoides renales humanos».
La investigadora destaca que las técnicas de microagregación e ingeniería genética empleadas permiten generar más de 30.000 organoides por cada placa de cultivo, «mientras que con otros métodos solo se obtenían unas decenas, de 20 a 50, en cada experimento». Esas cifras dan idea de la gran ventaja que aporta este hallazgo, pues acerca más la posibilidad de que en un futuro, se puedan incrementar los órganos viables para trasplante en las cantidades necesarias.
«Los organoides son estructuras de tamaño micrométrico», recuerda Elena Garreta, y carecen de vasos sanguíneos, por lo que no están listos para ser utilizados tal cual en un trasplante. Sin embargo, los investigadores buscan que «puedan ser usados para acondicionar y reparar órganos que ahora se descartan en los trasplantes. Acondicionar esos órganos antes del injerto ofrece la ventaja de poder aumentar el número de órganos viables y disminuir así la espera de pacientes crónicos para el trasplante», explica.
Para demostrarlo, han introducido organoides renales humanos en siete riñones de cerdo que se mantuvieron vivos fuera del organismo gracias a las máquinas de perfusión, con las que se mantienen los órganos oxigenados y condiciones fisiológicas adecuadas. «Aproximadamente se inyectaron 20.000 organoides por riñón. El número de organoides que se inyectaron se calculó sobre la base del peso del órgano», detalla Garreta.
El equipo constató que después de 24 y 48 horas del trasplante, los organoides humanos persistían integrados en el tejido renal porcino, mantenían su viabilidad y no desencadenaban ninguna respuesta inmune significativa. El riñón trasplantado continuaba funcionando con normalidad, y no se detectaron signos de daño ni toxicidad.
El experimento es un primer paso exitoso, al que deben seguir otros estudios. «En este trabajo no hemos evaluado la capacidad regenerativa del organoide en el riñón, porque el objetivo era determinar la viabilidad del procedimiento que hemos establecido, que se podía realizar con éxito y era seguro», aclara Garreta. Esperan continuar con nuevas investigaciones que confirmen que el órgano se regenera y el potencial terapéutico de estos organoides.
«Nuestra investigación demuestra que la combinación de tecnologías de organoides y perfusión ex vivo puede permitir intervenciones celulares en condiciones totalmente controladas», sintetiza Núria Montserrat sobre un trabajo multicéntrico, del que se destaca la colaboración con el INIBIC, la ONT y otras instituciones, como el Instituto de Salud Carlos III (ISCIII), para trasladar la investigación a un entorno quirúrgico realista y preclínico.
Rafael Matesanz, creador y fundador de la ONT, destaca a SMC que «probablemente, el mayor valor de este artículo es la descripción por vez primera de un método sistemático y escalable para producir estos organoides renales humanos en cantidades significativas y de una forma asequible, utilizando técnicas de microagregación e ingeniería genética. El procedimiento que aquí se describe puede tener una gran utilidad en investigaciones futuras». Y subraya que pueda «abrir la puerta a un procedimiento para reparar riñones y mejorar su viabilidad antes del trasplante».