Un ambicioso ensayo clínico en Reino Unido muestra que los pacientes que recibieron inyecciones en su cerebro de una proteína clave mejoraron claramente sus síntomas. Podría ser el primer paso para un nuevo tratamiento de la enfermedad.
Ha costado varios años de investigación y varios millones de libras, pero este miércoles se han conocido los resultados de un ambicioso ensayo clínico en humanos que trataba de observar los efectos de inyectar una proteína regeneradora de las células dopaminérgicas en el cerebro de los pacientes con la enfermedad de Parkinson. Los resultados muestran que después de 18 meses los pacientes presentan mejoras “de moderadas a grandes” en sus síntomas en comparación con la situación que presentaban antes del estudio. Y se abre la puerta a que este tipo de inyecciones consigan regenerar las células que el párkinson destruye en el cerebro de las personas que sufren la enfermedad.
Los resultados se presentan en dos trabajos publicados simultáneamente en las revistas Brain y Journal of Parkinson’s Disease y liderados por el investigador Alan Whone. Desde el año 2014, varios ensayos más modestos habían demostrado que la introducción del denominado Factor neurotrófico derivado de la glía (GDNF) producía mejoras significativas en los pacientes que se prolongaban durante varios meses. En los vídeos grabados por los autores – algunos de los cuales repiten en este estudio – se observaba una clara progresión de los enfermos después de recibir la inyección de esta proteína en zonas profundas de su cerebro.
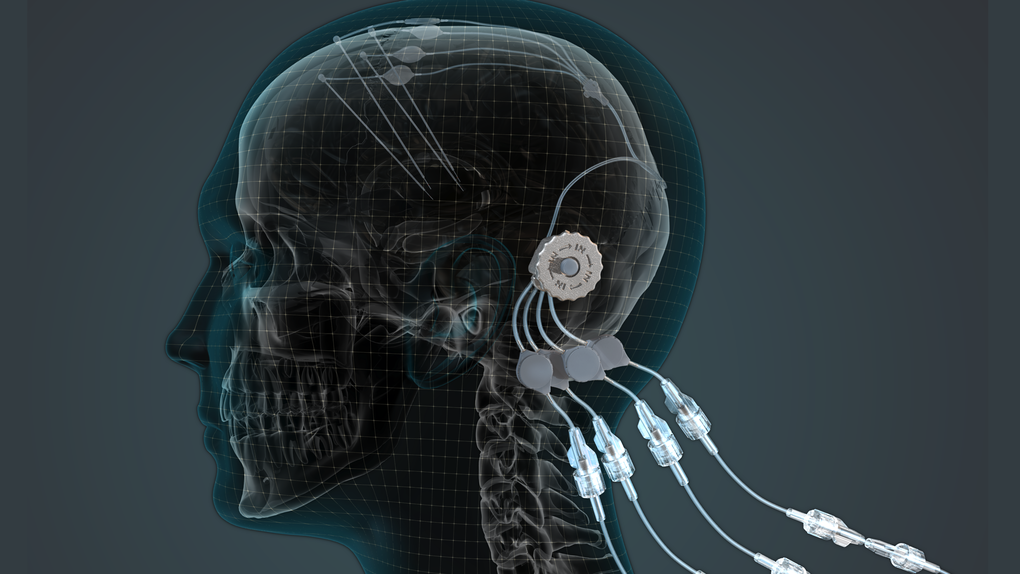
Para el ensayo que se publica ahora – financiado parcialmente por el sistema público de salud británico y varias fundaciones – se ha desarrollado un sistema especial para hacer llegar la proteína a las zonas del cerebro relacionadas con la producción de dopamina. Mediante cirugía robotizada se introdujeron cuatro tubos en la parte posterior de la cabeza de los participantes a través de los cuáles se podría suministrar el GDNF en una zona muy específica del cerebro.
“Este ensayo ha demostrado que podemos suministrar medicamentos de manera segura y continuada directamente en el cerebro de los pacientes durante meses o años mediante estos pequeños puertos implantados que sobresalen de la piel detrás de la oreja”, explica el neurocirujano Steven Gill, creador del dispositivo. El sistema es un avance importante dado que la mayoría de sustancias para este tipo de tratamientos solo se pueden inyectar con agujas, debido a que por vía sanguínea no pasarían la barrera hematoencefálica.
El ensayo se realizó mediante el sistema de “doble ciego” en 35 pacientes, de manera que una mitad recibió el tratamiento real y la otra un tratamiento placebo durante los primeros nueve meses. Después, por motivos éticos, se suministró la terapia real a todos los pacientes durante otros nueve meses. En un primer momento, y para decepción de los autores, no se apreciaron diferencias significativas entre los dos grupos, pero al realizar los escáneres cerebrales se vio una mejora “extremadamente prometedora” en el cerebro de quienes habían recibido la inyección de proteínas. Después de los primeros nueves meses el grupo de control no presentaba ningún cambio, pero los que recibieron una dosis de GDNF presentaban una mejora del cien por cien en una zona clave del cerebro afectada por la enfermedad, lo que abría la esperanza a que se estuvieran regenerando las células dañadas. Después de los 18 meses (cuando todos los participantes se incorporaron al tratamiento real) los dos grupos mostraban mejoras de moderadas a grandes en comparación con el principio del estudio.
Los autores reconocen que debido al diseño del ensayo les faltaría realizar más comprobaciones (las que no se pueden hacer por no dejar a un grupo sin tratamiento, algo que suele hacerse por motivos de humanidad en este tipo de ensayos). Aún así, creen que el resultado es altamente esperanzador para desarrollar un tratamiento de la enfermedad. “La magnitud espacial y relativa de la mejora que observamos en los escáneres cerebrales va más allá de lo que hemos visto en cualquier ensayo anterior”, asegura el doctor Whone. “Esto representa la prueba más convincente hasta ahora de que puede que tengamos una posible vía para despertar y restaurar células dopaminérgicas del cerebro que son progresivamente destruidas en el párkinson”.
“Durante el ensayo, noté una mejora en mi movilidad y mis niveles de energía, e incluso fui capaz de reducir mi medicación”, asegura Tom Phipps, uno de los participantes, de 63 años de edad. “Desde que acabó he aumentado mi medicación poco a poco, pero aún puedo montar en bicicleta, cavar en mi huerto y presidir el grupo local de Parkinson UK”. “Mientras los resultados no son tan claros como nos habría gustado”, añade Eric Mohr, miembro de MedGenesis, una de las empresas que financia el estudio, “cuando miras más de cerca hay signos prometedores para tratar el párkinson”. A José López Barneo, catedrático de Fisiología de la Universidad de Sevilla especialista en tratamiento con células madre que no ha participado en el ensayo, el estudio le parece un avance. “Ensayos previos de esta terapia fracasaron y ahora parece que se abren nuevas esperanzas”, asegura. “Los autores piensan que un tratamiento más prolongado y/o con mayor dosis del fármaco (el GDNF) podrían producir una mejoría clínica más manifiesta. En resumen, creo que los resultados de estos estudios son muy interesantes y prometedores”.